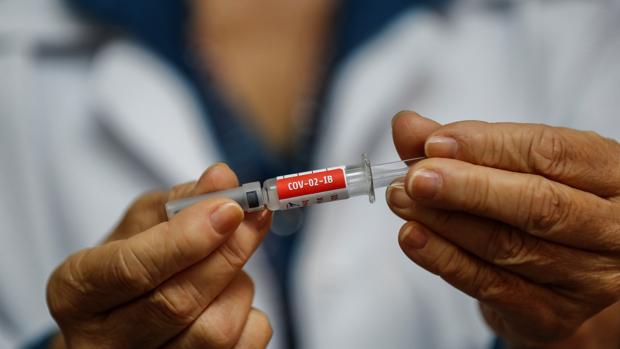
 El ministro de Sanidad, Salvador Illa, ha anunciado esta viernes que la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha autorizado el primer ensayo clínico de una vacuna en contra de el coronavirus en fase 2 en España, en otros términos, en humanos. Ésta es una de las 31 vacunas que ya se están probando en humanos, Conforme la Organización Mundial de la Salud (OMS). Aparte, otras 142 se aplican ya animales, cuatro de ellas en España. ¿Qué candidato a vacuna se marcha a sentir?
El ministro de Sanidad, Salvador Illa, ha anunciado esta viernes que la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha autorizado el primer ensayo clínico de una vacuna en contra de el coronavirus en fase 2 en España, en otros términos, en humanos. Ésta es una de las 31 vacunas que ya se están probando en humanos, Conforme la Organización Mundial de la Salud (OMS). Aparte, otras 142 se aplican ya animales, cuatro de ellas en España. ¿Qué candidato a vacuna se marcha a sentir?
Se probará la eficacia de un pretendiente a vacuna llamado Ad26.COV2-S, un fármaco que está siendo desarrollado por Janssen, filial de Johnson & Johnson, del que la empresa espera poder contar listas más de 1.000 millones de dosis en 2021. Este aspirante a medicamento consiste en un Sólo adenovirus atenuado (un tipo de virus que ha sido modificado para hacerlo menos peligroso) que funciona De esta forma como coche para introducir una proteína del SARS-CoV-2 en el cuerpo humano. ¿Es un candidato esencial?
«No es una vacuna cualquiera, es una vacuna preseleccionada por Europa y U.S.A. para sus posibles campañas de vacunación», ha explicado a ABC Jaime Jesús Pérez, vocal de la Asociación Española de Vacunología. «Está entre las seis vacunas elegidas por EE.UU. para formar comunicado de la intervención Warp Speed y También está entre las vacunas que la Comisión Europea ha negociado para su compra», ha añadido. Este pretendiente USA exactamente la misma tecnología que la vacuna Ad26.ZEBOV, ya aprobada frente el ébola, y También desarrollada por Janssen. a su vez, se U.S.A. en otras candidatos a vacunas en desarrollo frente a zika, VIH y virus respiratorio sincitial. «Es una tecnología muy novedosa Pero tremendamente prometedora y es exactamente la misma usada en la de AStra-Zeneca o bien vacuna de Oxford, por todos conocida». Esta semana, el Ministerio de Sanidad afirmó que España se había sumado a la compra de la Comisión Europea de esta vacuna y que las primeras dosis podrían llegar a comienzos de diciembre. ¿Cómo funciona?
Ad26.COV2-S transporta la datos genética necesaria para sintetizar la proteína S o proteína de la espícula del coronavirus, que es reconocida por el sistema inmunitario. De esta forma, En el momento en que el adenovirus se inyecta en el hombro, por poner un ejemplo, activa la producción de la proteína S en la zona, permitiendo que Ciertas células presenten esta molécula al sistema inmunitario. De esta manera, pasado un tiempo, las defensas se activan y pueden contestar de forma más rápida y eficaz en el horario se produzca el «ataque» del SARS-CoV-2. En teoría esta clase de vacuna podría incluso impedir la infección. ¿Qué se sabe Hasta el momento acerca de Ad26.COV2-S?
Ad26.COV2-S es un candidato que se ya ha probado en ensayos preclínicos, o bien sea, con animales. En concreto, se ha estudiado su seguridad y su capacidad de inducir la producción de anticuerpos neutralizantes en ensayos acontencimientos con macacos. ¿Qué quiere decir que son neutralizantes? Esencialmente, que los animales vacunados producen anticuerpos que bloquean al virus e impiden la infección de los pulmones, Según resumió un estudio publicado en «Nature» el 30 de julio. Un macaco parecido a los empleados en estudios con animales para este candidato a vacuna – Einar Fredriksen
Además, Desde el 10 de junio de 2020 Janssen tiene en marcha un ensayo que combina las fases 1 y 2 en el que se está estudiando la seguridad, la contestación a la vacunación y la inmunogenicidad del candidato en 1.045 voluntarios sanos, tanto en EEUU Al igual que en Bélgica. El 18 de agosto, se aprobó en Brasil un enorme estudio de fase 3, en el que se inyectará el pretendiente a 6.000 voluntarios, Sin embargo Johnson & Johnson planea ampliar el estudio y realizarlo De la misma forma en Argentina, Perú, Chile y México. ¿Dónde se van a hacer los ensayos?
Este aspirante será probado en un Sólo ensayo clínico en el que participarán un total de 190 voluntarios sanos de entre 18 y 55 años e mayores de 65, y cuyos primeros resultados se esperan en los cercanos meses. Dichas pruebas van a tener sitio en tres hospitales españoles: La Paz y La Princesa, en La capital española, y el Marqués De Valdecilla, en Santander. Paralelamente, el ensayo deberá sector en Alemania y Bélgica con otros 400 voluntarios. ¿Por qué en tantos lugares?
«El fin de hacer los ensayos en tantos lugares es contrarrestar el efecto de los sesgos», Según ha explicado a ABC Vicente Larraga, científico español que trabaja en el crecimiento de una vacuna ante el SARS-CoV2 y líder del Laboratorio de Parasitología Molecular del Centro de Investigaciones Biomédicas (CIB-CSIC). Tal También que ha expresado, se busca involucrar a investigadores de diferentes centros de salud para poseer unas conclusiones lo más objetivas posibles. Al mismo tiempo, al implicar a Múltiples centros se acelera la velocidad de reclutamiento de voluntarios. ¿Por qué se hacen experimentos con humanos?
Una vacuna es un medicamento diseñado para administrarse a millones de personas sanas. Por ello, se rige por los estándares de calidad más exigentes entre todos los medicamentos. Los ensayos preclínicos, en animales, y clínicos, en humanos, han de demostrar la calidad, seguridad y eficacia de estos fármacos. La Paz, en la imagen, es uno de los tres hospitales españoles donde se harán las pruebas con este pretendiente a vacuna – Guillermo Navarro
Ahora, Sólo para aprobar los ensayos de fase 2 ha hecho falta el visto bueno de la AEMPS y de Varios comités de moral. Esta aprobación ha llegado ahora de analizar los experimentos propuestos por Janssen, teniendo presente el diseño de los ensayos, las evidencias de estudios anteriores o la calidad del proceso de fabricación de los componentes. Llegado la situación de que esta vacuna se autorizase, sería necesaria la aprobación de la AEMPS y la Agencia Europea de Medicamentos (EMA por sus siglas en inglés). ¿Qué se hace en los ensayos de fase 2?
Esta etapa prosigue a los estudios preclínicos, en animales, y de fase 1, en humanos, en los que se inyecta el candidato a vacuna en decenas de voluntarios para estudiar la seguridad y la inmunogenicidad. Conforme ha explicado Vicente Larraga, los ensayos de fase 2 suelen involucrar a cientos de voluntarios sanos y durar uno o bien un par de años. En un caso así, la emergencia de alcanzar una vacuna acorta los plazos a unos dos meses. Estos ensayos están encaminados a determinar cuál es la dosis adecuada de vacuna que produce la contestación inmunitaria observada en la fase 1, a la vez que se hacen estudios de seguridad, No obstante ya partiendo de las garantías de la fase 1. Esta fase También puede sumar estudios de reto, en los que se infecta con el virus real a pacientes sanos previamente vacunados. «Esta es la etapa clave, la que prueba si la vacuna funciona o bien no» ha comentado Larraga. Es en ese punto En el momento en que se investiga «si la vacuna resguarda o no, si la carga viral disminuye y si hay menos afectación en los pulmones, por ejemplo», ha proseguido. Todo esto transcurre en un Ambiente controlado médicamente. ¿Qué se estudiará en este caso?
En el ensayo aprobado ahora se estudiará de qué manera calibrar la cantidad de dosis para generar la inmunidad, las diferencias entre administrar una o dos dosis, De esta manera Del mismo modo que el intervalo de tiempo que debería pasar entre dosis. A nivel de pruebas de laboratorio, se estudiará en qué grado se contrarresta al virus, cuántos anticuerpos se producen y la aparición de efectos secundarios. ¿Quién puede participar?
Según ha anunciado Salvador Illa, el reclutamiento de voluntarios empezará la semana procedente. La selección de voluntarios va a ser llevada a cabo por los centros hospitalarios En base a unos criterios especificados en el ensayo. Sanidad ha informado de que las solicitudes para contribuir se podrán entregar vía correo electrónico o bien llamando al celular de atención al cliente. A lo largo de estos ensayos se estudiará la contestación inmunitaria inducida por Múltiples dosis del candidato a vacuna en 190 voluntarios en España, y otros 400 en Bélgica y AlemaniaDe pacto a la datos proporcionada por la AEMPS, algunos de los criterios más importantes son: contar entre 18 y 55 años de edad, o 65 años en adelante inclusive. Estar sanos y no tener comorbilidades asociadas con un mayor riesgo de sufrir COVID-19 grave, Al idéntico que asma, enfermedades pulmonares, diabetes, afecciones cardíacas graves u obesidad. La única comorbilidad aceptada, y asociada con sufrir COVID-19 grave, es el tabaquismo. a su vez, serán excluidos quienes tengan una enfermedad aguda clínicamente significativa o fiebre, quienes tengan alergia a vacunas o bien un funcionamiento anómalo del sistema inmunitario, mujeres embarazadas o personas con hepatitis B o C. Por otra comunicado, tampoco podrán participar personas ya expuestas al SARS-CoV-2 ni trabajadores sanitarios que estén en contacto con infectados por este virus. ¿Es una ventaja para España contribuir?
El ministro de Sanidad ha puntualizado que participar en el estudio de esta vacuna no da a España ninguna ventaja en el reparto a nivel europeo: «Pero es un orgullo para nuestro país poder contribuir, desencadena conocimiento y reconocimiento a la calidad de nuestra investigación y a nuestro Sistema Nacional de Salud», ha argumentado. En opinión de Vicente Larraga, «la participación de España en este estudio de fase 2 no es algo extraordinario, Sino más bien un testimonio de la capacidad de nuestro sistema hospitalario». Tal Al semejante que ha comentado, España es un país en el que se llevan a cabo multitud de ensayos clínicos de esta naturaleza para otros medicamentos. ¿Cuándo podría estar lista esta vacuna?
La contestación dependerá de los resultados que se consigan en los ensayos en marcha. A la vez que avanzan los estudios, la empresa Johnson & Johnson trabaja en incrementar su capacidad de producción y en establecer acuerdos con otros socios para garantizar su acceso mundial. Según anunció, esperan contar la vacuna lista para la producción a principio de 2021. Johnson & Johnson ya ha cerrado un pacto de 1.000 millones de dólares con el gobierno de EEUU para suministrar 100 millones de dosis, y espera poder generar 1.000 millones para 2021.
